Магнитно резонансная протонная спектроскопия. Метод магнитно-резонансной (МР) спектроскопии головного мозга – что это такое. Электромагнитная совместимость с медицинской аппаратурой
Содержание
Метод магнитно-резонансной (МР) спектроскопии головного мозга – что это такое
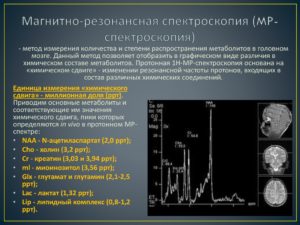
Протонная магнитно-резонансная спектроскопия – это развивающийся метод, способный выявлять заболевания головного мозга, сердечной мышцы посредством регистрации метаболического накопления глутамата, ацетилхолина, креатинина, ацетиласпартата и ряда других соединений. Сравнение активности веществ в норме и при патологии позволяет установить ранний диагноз, динамические оценить качество лечения через определенные временные промежутки.
Процедура МРТ головного мозга с МР спектроскопией – что это такое
Способ позволяет изучить функциональность головного мозга. Другие МР процедуры показывают анатомию органа. Сочетание функциональной и морфологической информации повышает информативность диагностики.
МР-спектроскопия позволяет изучить скорость движения молекул веществ, проводить дифференцировку разных тканей – серого и белого вещества, мышц, жира, крови.
Регистрация транспорта ионов калия, натрия через мембрану определяет активность фагоцитоза – уничтожения защитными клетками чужеродных агентов.
Сочатение с МРТ трактографией позволяет верифицировать состояние внутримозговых желудочков, перивентрикулярных пространств.Отслеживание накопления кислорода позволяет зарегистрировать участки повышенной возбудимости, выявить места разрушения гематоэнцефалического барьера, анализировать гормональную активность, проницаемость тканей.
Методы молекулярной нейровизуализации только развиваются – трактография, перфузионная диффузионная МРТ и МР-спектроскопия. Применяются обычно после нативной магнитно-резонансной томографии головного мозга. Только онкологи пользуются нейровизуализационными методами для оценки изменений мозговой ткани во время лечения опухолей.
Как делают протонную МР-спектроскопию
Неинвазивная МРТ головного мозга с МР спектроскопией разработана в 1951 году. Ученые использовали метод для регистрации измененной частоты протонов разных веществ под влиянием сильного магнитного поля.
Полувека наблюдения за атомами протонов ацетиласпартата, холина, миоинозитола, лактата, жировых соединений, глутамина позволило использовать информацию в медицине для выявления внутримозговых изменений, патологии сердечной мышцы.
Информативность имеют физиологические и патологические химические сдвиги соединений. Для примера, приводим протонный МР-спектр веществ в норме:
- Холин – 3,2 ppm;
- Ацетиласпартат – 2 ppm;
- Миоинозитол – 3,56 ppm;
- Жировые соединения – 1-1,2 ppm;
- Глутамат – 2,2-2,5 ppm;
- Креатинин – 3-3,9 ppm.
Инновационные разработки помогли совершенствовать метод. Существует 3 разновидности магнитно-резонансной спектроскопии:
- Одновоксельная;
- Мультивоксельная;
- Мультиядерная.
Разделение основано на регистрации протонных спектров одного или нескольких участков мозговой паренхимы одновременно. При одновоксельной МР-спектроскопии изучается единичный участок. Изучение спектров химического сдвига метаболитов заданной зоны помогает оценить биохимические процессы.
Мультивоксельный тип предполагает спектроскопический анализ разных сегментов. Подход применяется для оценки функциональности разных центров – чувствительных, двигательных, речи, слуха, зрения.
Мультиядерная МР спектроскопия оценивает химические сдвиги протонов углерода, фосфора, ряда других химических соединений одновременно. Распределение пиков повышает информативность исследования.
Информация анализируется путем просмотра параметрической карты среза. Каждый отдельный участок имеет несколько анатомических образований. Отслеживание биохимических спектров не позволяет дифференцировать ткань, но знание патофизиологии помогает предположить локализацию патологии.
Основные разработки МР-спектроскопии проводятся в области онкологии. С помощью процедуры нельзя предсказать тип новообразования. Наблюдения показали измененное соотношение метаболизма холина-креатинина, N-ацетиласпартата и креатина у большинства злокачественных образований. Некоторые раки сопровождаются повышением пика лактата.
Что показывает МР спектроскопия
Опробовано спектроскопическое обследование при верификации нейроэпителиальных опухолей, эпендимом, астроцитом. Метаболические сдвиги четко указывают тип новообразования.
Онкологи применяют МР-спектроскопию для диагностики наличия/отсутствия клеток образования после операционного удаления очага.
Обследования верифицирует признаки гибели злокачественной ткани после химиотерапии, лучевого облучения.
Динамический онкологический контроль лучше делать двумя методами – перфузионно-взвешенная МРТ в сочетании с 1 H-МР-спектроскопией. Подход выявляет участок некроза посредством обнаружения широкого протонного пика лактат-липидных соединений в пределах от 0,5 до 1,8 ппм. Одновременно прослеживается редукция сдвига других веществ, «мертвый пик».Очередная область использования спектроскопии – дифференциальная диагностика демиелинизирующих процессов (рассеянный склероз), инфекций, травматических повреждений.
Абсцессы мозга верифицируются по обнаружению спектров лейцина, валина, сукцината, липид-лактатного комплекса.
Литературные источники приводят информацию о возможности использования обследования для оценки метаболизма при черепно-мозговых травмах, эпилепсии, инсультах.
Контрастное МРТ головного мозга показывает состояние сосудов, верифицирует злокачественные и доброкачественные новообразования вначале развития.
Регистрация сдвигов валина, лейцина свидетельствует о распаде тканей при болезнях, бактериальных инфекциях. Продуктом бактериального гликолиза является накопление сукцината, ацетата. Изменение МР-спектров веществ позволяет предположить характер нозологии (органический, инфекционный, воспалительный).
Какие болезни выявляет протонная спектроскопия:
- Глиома изменяет пики распределения липидов, лактата, холина, креатинина, N-ацетиласпартата;
- Неглиальные новообразования сдвигают холин, ацетиласпартат;
- Инфаркты, инсульты регистрируются по повышению лактата, уменьшению других метаболитов;
- Инфекционные процессы приводят к повышению ацетата, аланина, лактата. Токсоплазмоз характеризуется снижением холина;
- Болезни белого вещества сопровождаются понижением миоинозитола, увеличением N-ацетиласпартата;
- Диагностика печеночной лейкоэнцефалопатии базируется на изучении увеличения глутамина, регистрации сниженного миоинозитола;
- Астроцитома разной степени злокачественности с локализацией в лобной доле при нативном МРТ характеризуется сигналом высокой силы. С помощью 2D мультивоксельной спектроскопии удается выявить повышение индекса холин/N-ацетиласпартата более единицы.
Цветное картирование дополняет информативность контрастной, нативной МР-томографии. Исследование имеет блестящие перспективы медицинского развития.
Источник: https://mrt-kt-golovnogo-mozga.ru/article/mrt-gm_spektroskopiya
Магнитно-резонансная спектроскопия. (МРС)

Суть метода заключается в спектральном анализе резонансных сигналов (резонансных частот) ряда атомов [фосфор (31Р), натрий (23Na), углерод (13С) и др.], входящих в состав соединений, осуществляющих важнейшие мозговые функции.
С помощью МРС можно получать количественную информацию о фундаментальных аспектах мозгового метаболизма и судить о характере нейрохимических процессов в мозге.
Протонная 1Н-МР-спектроскопия основана на «химическом сдвиге» — изменении резонансной частоты протонов, входящих в состав различных химических соединений. Термин ввел N. Ramsey в 1951 г., чтобы обозначить различия между частотами отдельных спектральных пиков.
Единица измерения «химического сдвига» — миллионная доля (ppm). Используется в исследованиях. Основные метаболиты и соответствующие им значения химического сдвига, пики которых определяются in vivo в протонном МР- спекгре, приведены в таблице 4.
Таблица 4.
Основные метаболиты и значения химического сдвига
| Метаболит | Аббревиатура | Химический сдвиг |
| N-ацетил аспартат | NAA | 2,0 ppm |
| Холин | Cho | 3,2 ppm; |
| Креатин | Сг | 3,03 и 3,94 ppm |
| Миоинозитол | ml | 3,56 ppm |
| Глутамат и глутамин | Glx | 2,1 -2,5 ppm |
| Лактат | Lac | 1,32 ppm |
| Липидный комплекс | Lip | 0,8-1,2 ppm |
В настоящее время в протонной МР-спектроскопии используют два основных метода — одновоксельную и мультивоксельную (Chemical shift imaging) МР-спектроскопию — единовременное определение спектров от нескольких участков головного мозга.
В практику сейчас стала также входить мультиядерная МР- спектроскопия на основе МР-сигнала ядер фосфора, углерода и некоторых других соединений. При одновоксельной 1НМР-спектроскопии для анализа выбирают только один участок (воксел) мозга.
Анализируя состав частот в регистрируемом от этого воксела сигнале, получают распределение пиков метаболитов по шкале химического сдвига (ppm).
Соотношение между пиками метаболитов в спектре, уменьшение или увеличение высоты отдельных пиков спектра позволяют неинвазивно оценивать биохимические процессы, происходящие в тканях. Распределение метаболита N-ацетиласпартата в головном мозге представлено на рисунке 7.Рис.7. Распределение метаболита N-ацетиласпартата в головном мозге
N-ацетиласпартат, или N-ацетил аспартат (NAA) (англ. N-acetyl aspartate, N-acetylaspartate, N-acetyl-L-aspartate, N-acetylaspartic acid),— производное аспарагиновой кислоты, имеет формулу C6H9N05 и молекулярный вес 175,139 г/моль. В больших количествах содержится в тканях мозга, составляет 1 % его сухого веса и отвечает за 3—4 % его суммарной осмолярности [Baslow М.Н., 2000].
Концентрация в мозге составляет 6—7 нмоль/г и в этом N-ацетиласпартат уступает лишь глутамату. Несмотря на это, сам факт наличия N-ацетиласпартата в мозге был установлен лишь в 1956 году X. Талланом [Tallan Н.Н., Moore S, Stein WH., 1956]. Подавляющая доля содержащегося в мозге NAA синтезируется митохондриями нейронов из ацетил-кофермента А при помощи аспартат-N- ацетилтрансферазы[Т8а1 G.
, Coyle J.T., 1995]. Снижение уровня NAA считается достоверным индикатором нейрональной дисфункции и гибели нейронов [Fukuzako Н, Takeuchi К, Hokazono Y et al, 1995]. Например, при МРС — исследованиях больных шизофренией отмечаются локализованные зоны недостаточности N-ацетил аспаргата в префронтальной коре, височных долях, гиппокампе [Deicken RF, Johnson С, Pegues М., 2000; AbAbbott C.
, Bustillo J., 2006].
Показано, что сокращение количества NAA в префронтальном кортек- се при хронической шизофрении связано со снижением когнитивных способностей, большей продолжительностью болезни и ухудшением негативной симптоматики.
Снижение уровня NAA происходит в областях мозга, претерпевающих потерю нейронов, также может свидетельствовать об ослаблении нейронального метаболизма или о нарушении процесса миелинизации нервных волокон. Эта патология может являться причиной обнаруживаемых при шизофрении нарушений работы префронтальной коры.
[Wood S.J, Berger G., Velakoulis D., et al. 2003; Mondino M, Brunelin J., Saoud ML, 2013].
Позитронная эмиссионная томография (ПЭТ) — метод прижизненного изучения обменных процессов в ткани головного мозга с возможностью одновременного получения данных о мозговом кровотоке.
Он основывается на использовании феномена позитронной эмиссии, происходящей во введенном в организм меченном радиоизотопами веществе при его распределении и накоплении в мозговых структурах. Для изучения мозгового метаболизма используются следующие изотопы: l8F, ПС, 13N или 150 (чаще всего используется радиоактивно меченная глюкоза).
Для исследования регионального мозгового кровотока чаще применяют 150 (маркированная вода) или инертный газ 18F — флюорметан. Соответствующее вещество, будучи введенным в организм, с током крови распределяется по органам, достигает мозга и излучаемые им позитроны улавливаются детекторами (ПЭТ-камерами), которые расположены кольцеобразно вокруг головы.
Изотопы накапливаются, прежде всего, в сером веществе, где плотность нейронов наиболее высокая — в коре, базальных ганглиях, таламусе и мозжечке. Изменения в накоплении изотопов в какой-либо области мозга позволяют предполагать нарушение нейрональной активности.Подобным же образом могут прослеживаться пути лигандов нейрорецепторов, белков обратного захвата (reuptake proteins), лекарственных препаратов. ПЭТ обеспечивает изображение функционального состояния мозга и является особенно многообещающим методом при исследовании ней- ротрансмиттерных систем.
Химические элементы (кислород, углерод и азот) с коротким периодом полураспада и излучающие позитроны используются в качестве метки органических соединений (например, глюкозы, аминокислот и нейромедиаторов). Последние вводятся в организм с помощью инъекции или ингаляции. Затем картируется распределение этого вещества в разных отделах мозга.
С помощью ПЭТ можно визуализировать картину мозгового кровотока, выявлять определенные нейрогрансмиттерные системы головного мозга, in vivo оценивать характер мозгового метаболизма (например, глюкозы). Существенным преимуществом этого метода является его способность обнаруживать мозговую патологию на функциональном уровне до этапа грубых органических нарушений.
С помощью ПЭТ обнаружено снижение функциональной активности лобных долей при шизофрении. Метод дает сведения о локализации дофаминовых рецепторов, что важно в изучении новых антипсихотиков.
Позитронноэмиссионные томографы последних моделей могут одновременно определять и подсчитывать показатели различных метаболических процессов, по меньшей мере, на 15 аксиальных мозговых срезах при минимальном размере участка среза 5—6 мм. При проведении ПЭТ нередко используются психологические тесты, позволяющие определить особенности функционирования различных областей мозга. Комбинация ПЭТ с МРТ дает возможность уточнить анатомическую локализацию региональных функциональных параметров мозга, способствует пониманию функционально-морфологических связей. Характеристика уровня метаболизма при обсессивно-компульсивном расстройстве в сравнении с нормой представлена на рисунке 8.
Рис. 8. Картина ПЭТ в норме и при обсессивно-компульсивном расстройстве (Аткинсон Р. Л. и др., 2003).
При исследовании мозга человека было обнаружено, что префронтальная кора некоторых людей, страдающих шизофренией, меньше по размерам и менее активна, чем у нормальных индивидов (рис. 9).
Префронтальная кора является наиболее крупным участком мозга у людей, составляя около 30% всей коры головного мозга и связанной со всеми остальными кортикальными зонами, с лимбической системой, ответственной за эмоции и когнитивную деятельность, а также с базальными ганглиями, ответственными за моторные движения.Префронтальная кора играет важную роль в возникновении речи, выражении эмоций; планировании и формировании новых идей, а также в опосредовании социальных взаимодействий.
Таким образом, логично предположить, что у людей со значительно уменьшенной в размерах или менее активной префронтальной корой могут встречаться различные нарушения в когнитивной, эмоциональной и социальной сфере, как это имеет место у лиц, страдающих шизофренией [Аткинсон Р. Л. и др., 2003].
Рис. 9. ПЭТ-сканер показывает разницу в уровне метаболизма между участками мозга у больного шизофренией и у нормального человека (по Аткинсон Р.Л, Аткинсон Р.С, Смит Э.Е, Бем Д. Дж. и др., 2003 ).
Применение ПЭТ, однако, имеет ограничения для его широкого применения не только в клинических, но и научных исследованиях, так как он требует дорогостоящего оборудования, включающего атомный реактор (используемые радиоизотопы являются корогкоживущими и должны изготовляться на месте их применения). Поэтому исследования с применением ПЭТ имеют возможность проводить лишь немногие научные центры.
Page 3
Однофотонная эмиссионная томография (ОФЭТ) позволяет получать информацию о региональном мозговом кровотоке.
При исследовании в кровь вводятся испускающие фотоны радионуклиды, которые после их прохождения через гематоэнцефалический барьер (ГЭБ) обнаруживаются вращающейся вокруг головы гамма-камерой либо кольцевыми детекторами.
В качестве изотопов используют радиоактивные газы криптон (85Кг) или ксенон (|33Хе), а в последнее время — гексаметил- пропиленаминоксин (ГМПАО).
Локализация введенных радиоизотопов в заданном поперечном слое мозга определяется в первую очередь мозговым кровотоком, поэтому ОФЭТ может оценивать изменения кровотока в различных (корковых и глубинных) областях мозга в норме и при патологии, в том числе и при функциональной нагрузке, например, в условиях психологического эксперимента. ОФЭТ уступает ПЭТ по информативности, но гораздо экономичнее и может использоваться в клинической практике.
— малоинвазивный МРТ-метод — с минимальной инвазивностью, высокой чувствительностью в оценке тканевой микроциркуляции, высокой разрешающей способностью, коротким временем исследования.
Есть методы исследования гемодинамических перфузионных процессов с помощью экзогенных и эндогенных маркёров (с использованием контрастных веществ; получение изображений, зависящих от уровня оксигенации крови, др.). Перфузионной МРТ называют методы оценки перфузии при прохождении болюса контрастного вещества.Эти методы исследования мозговой перфузии наиболее широко применяют в МР- диагностике, особенно в сочетании с диффузионными исследованиями. По мере прохождения болюса контрастного вещества по сосудистой системе многократно регистрируют изображение одного и того же среза (обычно это 10 разных уровней или срезов). Сканирование занимает 1-2 мин.
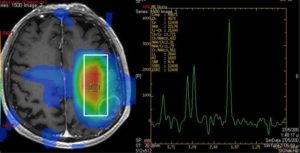
График снижения интенсивности МР-сигнала даёт зависимость «интенсивность сигнала — время» в каждом пикселе среза. Форма этой кривой в артерии и вене определяет артериальную и венозную функции, с помощью которых рассчитывают гемодинамические тканевые параметры (рисунок 10).
Рис. 10. Срезы головного мозга, получаемые при МР-перфузии.
Источник: https://bstudy.net/611604/estestvoznanie/magnitno_rezonansnaya_spektroskopiya
Яичник холин креатинин протонная магнитно резонансная спектроскопия. Магнитно-резонансная томография
За их открытия, касающиеся метода МРТ. Однако вручению этой премии сопутствовал скандал, как бывало в ряде случаев, по поводу авторства открытия .
В создание магнитно-резонансной томографии известный вклад внёс также американский учёный армянского происхождения Реймонд Дамадьян , один из первых исследователей принципов МРТ, держатель патента на МРТ и создатель первого коммерческого МРТ-сканера.
В 1971 году он опубликовал свою идею под названием «Обнаружение опухоли с помощью ядерного магнитного резонанса». Имеются сведения, что именно он изобрёл само устройство МРТ . Кроме того, ещё в 1960 году в СССР изобретатель В. А.
Иванов направил в Комитет по делам изобретений и открытий заявку на изобретение, где по появившимся в начале 2000-х годов оценкам специалистов были подробно обозначены принципы метода МРТ .
Однако авторское свидетельство «Способ определения внутреннего строения материальных объектов» № 1112266 на эту заявку, с сохранением даты приоритета её подачи, было выдано В. А. Иванову только в 1984 году .
Используемое в методе МРТ явление ядерного магнитного резонанса (ЯМР) известно с 1938 года.
Первоначально применялся термин ЯМР-томография, который после Чернобыльской аварии в 1986 году был заменён на МРТ в связи с развитием радиофобии у людей.
В новом названии исчезло упоминание о «ядерном» происхождении метода, что и позволило ему войти в повседневную медицинскую практику, однако используется и первоначальное название.
Томография позволяет визуализировать с высоким качеством головной, спинной мозг и другие внутренние органы.
Современные технологии МРТ делают возможным неинвазивно (без вмешательства) исследовать работу органов — измерять скорость кровотока, тока спинномозговой жидкости, определять уровень диффузии в тканях, видеть активацию коры головного мозга при функционировании органов, за которые отвечает данный участок коры (функциональная магнитно-резонансная томография — фМРТ).
Метод
Аппарат для магнито-резонансной томографии
Метод ядерного магнитного резонанса позволяет изучать организм человека на основе насыщенности тканей организма водородом и особенностей их магнитных свойств, связанных с нахождением в окружении разных атомов и молекул.
Ядро водорода состоит из одного протона , который имеет спин и меняет свою пространственную ориентацию в мощном магнитном поле, а также при воздействии дополнительных полей, называемых градиентными, и внешних радиочастотных импульсов, подаваемых на специфической для протона при данном магнитном поле резонансной частоте. На основе параметров протона (спинов) и их векторных направлений, которые могут находиться только в двух противоположных фазах, а также их привязанности к магнитному моменту протона можно установить, в каких именно тканях находится тот или иной атом водорода. Иногда могут также использоваться МР-контрасты на базе гадолиния или оксидов железа .
Если поместить протон во внешнее магнитное поле, то его магнитный момент будет либо сонаправлен, либо противоположно направлен магнитному полю, причём во втором случае его энергия будет выше.
При воздействии на исследуемую область электромагнитным излучением определённой частоты часть протонов поменяют свой магнитный момент на противоположный, а потом вернутся в исходное положение.При этом системой сбора данных томографа регистрируется выделение энергии во время релаксации предварительно возбуждённых протонов.
Первые томографы имели индукцию магнитного поля 0,005 Тл , и качество изображений, полученных на них, было низким. Современные томографы имеют мощные источники сильного магнитного поля. В качестве таких источников применяются как электромагниты (обычно до 1-3 Тл, в некоторых случаях до 9,4 Тл), так и постоянные магниты (до 0,7 Тл).
При этом, так как поле должно быть весьма сильным, применяются сверхпроводящие электромагниты, работающие в жидком гелии , а постоянные магниты пригодны только очень мощные, неодимовые .
Магнитно-резонансный «отклик» тканей в МР-томографах на постоянных магнитах слабее, чем у электромагнитных, поэтому область применения постоянных магнитов ограничена.
Однако постоянные магниты могут быть так называемой «открытой» конфигурации, что позволяет проводить исследования в движении, в положении стоя, а также осуществлять доступ врачей к пациенту во время исследования и проведение манипуляций (диагностических, лечебных) под контролем МРТ — так называемая интервенционная МРТ.
Для определения расположения сигнала в пространстве, помимо постоянного магнита в МР-томографе, которым может быть электромагнит, либо постоянный магнит, используются градиентные катушки, добавляющие к общему однородному магнитному полю градиентное магнитное возмущение.
Это обеспечивает локализацию сигнала ядерного магнитного резонанса и точное соотношение исследуемой области и полученных данных. Действие градиента, обеспечивающего выбор среза, обеспечивает селективное возбуждение протонов именно в нужной области.
Мощность и скорость действия градиентных усилителей относится к одним из наиболее важных показателей магнитно-резонансного томографа. От них во многом зависит быстродействие, разрешающая способность и соотношение сигнал/шум.
Современные технологии и внедрение компьютерной техники обусловили возникновение такого метода, как виртуальная эндоскопия , который позволяет выполнить трёхмерное моделирование структур, визуализированных посредством КТ или МРТ.Данный метод является информативным при невозможности провести эндоскопическое исследование, например, при тяжёлой патологии сердечно-сосудистой и дыхательной систем.
Метод виртуальной эндоскопии нашёл применение в ангиологии , онкологии , урологии и других областях медицины.
Результаты исследования сохраняются в лечебном учреждении в формате DICOM и могут быть переданы пациенту или использованы для исследования динамики лечения.
До и во время процедуры МРТ
Перед сканированием требуется снять все металлические предметы, проверить наличие татуировок и лекарственных пластырей . Продолжительность сканирования МРТ составляет обычно до 20-30 минут, но может продолжаться дольше. В частности, сканирование брюшной полости занимает больше времени, чем сканирование головного мозга.
Так как МР томографы производят громкий шум, обязательно используется защита для ушей (беруши или наушники) . Для некоторых видов исследований используется внутривенное введение контрастного вещества .
Перед назначением МРТ пациентам рекомендуется узнать: какую информацию даст сканирование и как это отразится на стратегии лечения, имеются ли противопоказания для МРТ, будет ли использоваться контраст и для чего. Перед началом процедуры: как долго продлится сканирование, где находится кнопка вызова и каким способом можно обратиться к персоналу во время сканирования .
МР-диффузия
МР-диффузия — метод, позволяющий определять движение внутриклеточных молекул воды в тканях.
Диффузионно-взвешенная томография
В частности, существуют специальные характеристики, указывающие на скоростной и объёмный приток крови, проницаемость стенок сосудов, активность венозного оттока, а также другие параметры, которые позволяют дифференцировать здоровые и патологически изменённые ткани:
- Прохождение крови через ткани мозга
- Прохождение крови через ткани печени
Метод позволяет определить степень ишемии головного мозга и других органов.
МР-спектроскопия
Магнитно-резонансная спектроскопия (МРС) — метод, позволяющий определить биохимические изменения тканей при различных заболеваниях по концентрации определённых метаболитов.
МР-спектры отражают относительное содержание биологически активных веществ в определённом участке ткани, что характеризует процессы метаболизма .
Нарушения метаболизма возникают, как правило, до клинических проявлений заболевания, поэтому на основе данных МР-спектроскопии можно диагностировать заболевания на более ранних этапах развития.
Виды МР спектроскопии:
- МР спектроскопия внутренних органов (in vivo)
- МР спектроскопия биологических жидкостей (in vitro)
МР-ангиография
Артерии головного мозга
Магнитно-резонансная ангиография (МРА) — метод получения изображения просвета сосудов при помощи магнитно-резонансного томографа . Метод позволяет оценивать как анатомические, так и функциональные особенности кровотока.
МРА основана на отличии сигнала от перемещающихся протонов (крови) от окружающих неподвижных тканей, что позволяет получать изображения сосудов без использования каких-либо контрастных средств — бесконтрастная ангиография (фазово-контрастная МРА и время-пролетная МРА).
Для получения более чёткого изображения применяются особые контрастные вещества на основе парамагнетиков (гадолиний).
Функциональная МРТ
Функциональная МРТ (фМРТ) — метод картирования коры головного мозга, позволяющий определять индивидуальное местоположение и особенности областей мозга, отвечающих за движение, речь, зрение, память и другие функции, индивидуально для каждого пациента.
Суть метода заключается в том, что при работе определённых отделов мозга кровоток в них усиливается.
В процессе проведения ФМРТ больному предлагается выполнение определённых заданий, участки мозга с повышенным кровотоком регистрируются, и их изображение накладывается на обычную МРТ мозга.
Мрт позвоночника с вертикализацией (осевой нагрузкой)
Методика исследования пояснично-крестцового отдела позвоночника — МР-томография с вертикализацией. Суть исследования состоит в том, что сначала проводится традиционное МРТ-исследование позвоночника в положении лежа, а затем производится вертикализация (подъём) пациента вместе со столом томографа и магнитом.
При этом на позвоночник начинает действовать сила тяжести, а соседние позвонки могут сместиться друг относительно друга и грыжа межпозвонкового диска становится более выраженной. Также этот метод исследования применяется нейрохирургами для определения уровня нестабильности позвоночника с целью обеспечения максимально надёжной фиксации.
В России пока это исследование выполняется в единственном месте.
Измерение температуры с помощью МРТ
МРТ-термометрия — метод, основанный на получении резонанса от протонов водорода исследуемого объекта. Разница резонансных частот даёт информацию об абсолютной температуре тканей. Частота испускаемых радиоволн изменяется с нагреванием или охлаждением исследуемых тканей.
Эта методика увеличивает информативность МРТ исследований и позволяет повысить эффективность лечебных процедур, основанных на селективном нагревании тканей. Локальное нагревание тканей используется в лечении опухолей различного происхождения .
Электромагнитная совместимость с медицинской аппаратурой
Сочетание интенсивного магнитного поля, применяемого при МРТ-сканировании, и интенсивного радиочастотного поля предъявляет экстремальные требования к медицинскому оборудованию, используемому во время исследований. Оно должно иметь специальную конструкцию и может иметь дополнительные ограничения по использованию вблизи установки МРТ.
Противопоказания
Существуют как относительные противопоказания, при которых проведение исследования возможно при определённых условиях, так и абсолютные, при которых исследование недопустимо.
Абсолютные противопоказания
- установленный кардиостимулятор (изменения магнитного поля могут имитировать сердечный ритм)
- ферромагнитные или электронные имплантаты среднего уха
- большие металлические имплантаты, ферромагнитные осколки
- ферромагнитные аппараты Илизарова .
Относительные противопоказания
Дополнительным противопоказанием для МРТ является наличие кохлеарных имплантатов — протезов внутреннего уха. МРТ противопоказана при некоторых видах протезов внутреннего уха, так как в кохлеарном имплантате есть металлические части, которые содержат ферромагнитные материалы.
Если МРТ выполняется с контрастом, то добавляются следующие противопоказания:
Примечания
- ISBN 978-0-521-86527-2 глава 8 Getting in tune: resonance and relaxation
- Филонин О. В. Общий курс компьютерной томографии / Самарский научный центр РАН. — Самара, 2012. — 407 с. — ISBN 978-5-93424-580-2 .
- Lauterbur P.C. Image Formation by Induced Local Interactions: Examples of Employing Nuclear Magnetic Resonance (англ.) // Nature : journal. — 1973. — Vol. 242, no. 5394. — P. 190-191. — DOI :10.1038/242190a0 . — Bibcode : 1973Natur.242..190L.
- Изобретение МРТ | Марина Собе-Панек (рус.) (неопр.) . sobepanek.com. Дата обращения 5 февраля 2018.
- Реймонд Ваган Дамадьян, учёный и изобретатель (неопр.) . 100lives.com. Дата обращения 25 мая 2015.
- The Nobel Prize vs. the Truth of History (англ.). fonar.com. Дата обращения 12 мая 2015.
- MacWilliams B. Russian claims first in magnetic imaging (англ.) // Nature: journal. — 2003. — November (vol. 426, no. 6965). — P. 375. — DOI :10.1038/426375a . — Bibcode : 2003Natur.426..375M. — PMID 14647349 .
- Татьяна БАТЕНЕВА. Привет Нобелю от Иванова: Как советский лейтенант-ракетчик перегнал Америку // Известия науки. 27.10.2003.
- Патенты Иванова Владислава
- Иванов В. А. Патент № 1112266. Способ определения внутреннего строения материальных объектов
- Иванов В. А.
Источник: https://edema-club.ru/pregnant/yaichnik-holin-kreatinin-protonnaya-magnitno-rezonansnaya-spektroskopiya/
Магнитно-резонансная спектроскопия

Магнитно-резонансную томографию давно используют во всех областях медицинской науки, поскольку данный вид обследования является безопасным и высокоинформативным для врачей при определении патологий и определения методик лечения пациентов.
Однако бывают ситуации, когда даже такое информативное исследование не позволяет точно выявить все аспекты заболевания. В таких ситуациях проводятся дополнительные исследования, которые в своей сути так же основываются на ядерно-магнитном резонансе.
Важнейшей из таких специализированных методик является магнитно-резонансная спектроскопия.
Суть исследовательской методики
Современные исследовательские клиники проводят магнитно-резонансную спектроскопию с применением специализированного оборудования. Такой метод исследования определяет биохимические изменения, которые вызываются различными патологическими состояниями, в разных участках человеческого организма.
Протонная магнитно-резонансная спектроскопия основывается на изменениях резонансной частоты протонов, из которых состоят всевозможные химические соединения. Такой процесс в медицине принято называть химическим сдвигом, что определяет различия частот пиков спектра.
Единицей измерения химического сдвига принято считать миллионную долю (ррт). На сегодняшний день протонная магнитно-резонансная спектроскопия подразделяется на ту, что проводится по одновоксельной методике, и мультивоксельную, которая может одномоментно определять спектры из нескольких участков головного мозга.
В современной медицине применяется еще одна разновидность спектроскопии – мультиядерная, учитывающая магнитно-резонансные сигналы фосфорных, углеродных и некоторых иных ядер.
При одновоксельной магнитно-резонансной спектроскопии анализу подлежит лишь один воксел или участок мозга человека.
При анализе состава частот спектра выбранного воксела специалисты получают определенное метаболитное распределение химического сдвига в миллионных долях.
При этом по соотношению в спектре метаболитных пиков, уменьшению или увеличению их высот можно неинвазивным путем оценить протекающие в тканях биохимические процессы.
Мультивоксельная спектроскопия предоставляет спектральные значения сразу нескольких необходимых при исследовании вокселов, которые можно сравнить для получения целостности картины исследуемого участка.
Данные мультивоксельной магнитно-резонансной спектроскопии позволяют строить карту среза по параметрам, где цветовыми маркерами обозначены концентрации необходимых метаболитов, а распределенность метаболитов в срезе визуализирована и предоставляет взвешенное по параметру химического сдвига изображение.По характеру исследуемых тканей магнитно-резонансная спектроскопия может подразделяться на:
- МР-спектроскопию, которая проводится на внутренних органах;
- МР-спектроскопию, областью исследования которой выступает биологическая жидкость.
Наиболее частым спектром применения методики выступает анализ мышечной ткани, поскольку она не подлежит ни одному другому неинвазивному методу диагностики и может быть обследована только путем применения биопсии.
Области применения диагностики
Рассматриваемая диагностика позволяет расшифровывать процессы метаболизма тканей различных органов при помощи получаемых магнитно-резонансных спектров. Обменные процессы организма, в большинстве случаев, нарушаются гораздо раньше, чем пациент начинает ощущать какие-то симптомы того или иного заболевания.
Вот почему важно своевременно применять магнитно-резонансную спектроскопию, которая поможет выявить отклонения на ранних стадиях болезни и принять соответствующие меры по предотвращению ее прогрессирования. К тому же, данная методика для отдельных анатомических областей организма человека является единственной неинвазивной диагностической процедурой, которая известна на сегодняшний день.
Для диагностики энергетического показателя метаболического процесса сердечной мышцы без введения радиоактивных средств магнитно-резонансная спектроскопия является единственно возможным методом обследования.
При сочетании методики с результатами магнитно-резонансной томографии врач получает общую клиническую картину кардиологических параметров – размеров сердца, структуры миокарда и нарушений кровообращения в нем, функциональных расстройств. Также вышеназванная диагностика помогает контролировать ход лечения ишемической болезни сердца, различной гипертрофии, сердечной недостаточности.
При неврологических патологиях магнитно-резонансная спектроскопия позволяет уточнить диагноз, различая, например, рассеянный склероз и нейрооптикомиелит. При расстройствах психики важным является та особенность данной диагностики, которая помогает рассмотреть различные биохимические процессы в мозговых клетках.
Данная методика широко применима для оценивания всевозможных новообразований в головном мозге.
Несмотря на отсутствие гистологических данных о возникшем новообразовании, исследователи говорят об определенных соотношениях рассматриваемых в ходе диагностики показателей и возникновении пика лактата.Таким образом, большинство случаев магнитно-резонансной спектроскопии опухолевых тканей способно предоставить дифференциацию возникших новообразований по принципу злокачественности.
В клинических условиях при послеоперационных диагностиках данная методика свидетельствует об успешности проведенного хирургического вмешательства либо о продолжении роста рассматриваемой опухоли, ее рецидиве, лучевом некрозе.
Еще одним аспектом использования магнитно-резонансной спектроскопии является процесс разграничения впервые обнаруженных первичных или вторичных патологий, их дифференциация по демиелинизирующим и инфекционным процессам.
Показательными являются в данном разрезе диагностированные случаи абсцессов, опирающиеся на диффузионно-взвешенные изображения.
Так, при отсутствующих пиках основных метаболитов при абсцессе отмечается возникновение пиков липид-лактатного комплекса и специфичных абсцессу пиков – например, продуктов анаэробного бактериального гликолиза и результатов протеолиза.
В медицинских источниках часто исследуется эффективность МР-спектроскопии при метаболических нарушениях и дегенеративных поражениях белого вещества мозга у детей, эпилепсии, черепно-мозговых травмах, ишемиях головного мозга и прочих заболеваниях.
Показания и противопоказания для МРС
Рассматриваемая диагностика, аналогично магнитно-резонансной томографии, основана на ядерно-магнитном резонансе, но ее результатом не выступают снимки.
Методика помогает рассматривать правильность распределения в тканях продуктов метаболических процессов, основываясь на их молекулярных особенностях.
Среди основных состояний и заболеваний, при которых пациентам показано прохождение магнитно-резонансной спектроскопии, выделяют эпилепсию, ишемическую болезнь (местное малокровие), болезни Альцгеймера и Паркинсона, всевозможные воспалительные процессы, травмирование тканей, возникновение новообразований в головном мозге.
Поскольку метаболизм здоровых и пораженных тканей значительно отличается, проведение данного вида исследования помогает диагностировать и начать лечить проблему на самой ранней стадии, что чаще приводит к успешному результату.Среди главных противопоказаний к процедуре специалисты называют искусственный водитель ритма. В случае наличия протезирования внутреннего уха либо искусственного сердечного клапана важно своевременно информировать об этом врача и предоставить ему подробное описание или аннотацию имеющегося протеза.
Также, поскольку исследование проводится в закрытом пространстве – продолговатой кабине, при наличии боязни таких пространств необходимо сообщить об этом специалисту, чтобы он мог прописать пациенту седативные (успокоительные) препараты.
Методика исследования, описанная выше, является многообещающей, поскольку при ее сочетании с другими обследованиями точность поставленного диагноза обычно достигает 90%. Иногда случаются неточности в связи с особенностью опухолевой ткани, которая может не сильно отличаться от нормальной по содержанию холина и степени зрелости.
В остальных случаях данное исследование очень информативно показывает специалистам, что происходит с обследуемым участком.
Источник: https://FoodandHealth.ru/diagnostika/magnitno-rezonansnaya-spektroskopiya/